√100以上 ナトリウム 水 反応 979275-ナトリウム 水 反応 エネルギー
水酸化ナトリウム液は、リトマス紙で調べると、赤→青色に変化する、アルカリ 性の すいようえき 水溶液の代表ともいえます。 水酸化ナトリウム液に、スチールウール(糸のように細くした鉄)や細い 水酸化ナトリウムと塩酸が反応すると塩化ナトリウムが発生しますが、この反応について教えてください。 ナトリウムイオンはなぜ、水酸化物イオンとの結合をやめて塩素と引っ付くのでしょうか? / ナトリウムイオンはなぜ、水酸化物イオンとの結合をやめて塩素と引っ水酸化ナトリウム と反応して 炭酸ナトリウム を与える。

アルミニウムと水酸化ナトリウム水溶液の反応 化学がちょっとだけ好きな社労士
ナトリウム 水 反応 エネルギー
ナトリウム 水 反応 エネルギー-食品添加物 (8)亜硝酸ナトリウム(NaNO2)の反応性 (A) 亜硝酸ナトリウム(NaNO 2 ) のイオン化 亜硝酸ナトリウムを水に溶かすと、亜硝酸ナトリウムは塩(えん)なので、水に溶けやすい性質がありますから、次の様にイオン化します。もんじゅでナトリウム水反応が起きる可能性のある部分は何処? もんじゅでは冷却水としてナトリウムを採用しています。 ナトリウムー水反応が起きる部分はどこになるのでしょうか? 原子力発電のしくみは、水を加熱し、水蒸気を使ってタービン




4 10ml 73ml Descubre Como Resolverlo En Qanda
ナトリウムは空気中の水蒸気と活発に発熱反応する21 ナトリウムを微粒化して液体のパラフィン系炭化水素中に (2) 日本燃焼学会誌 第45巻133号 (03年) 表1 ナトリウムの主な物性11 数値等 単位 備考 '子 Na 周期表族 Ia 電子配列 1s2 銀 2 白 2p'色,6381 外見すなわち、ナトリウム Na の方が、カルシウム Ca よりも激しく水 H 2 O と反応するのです。 カルシウム Ca とナトリウム Na を比べたとき、昇華熱 Q 1 とイオン化エネルギー Q 2 こそ、 Ca > Na でナトリウム Na が有利ですが、水和熱 Q 3 は、 Ca >> Na でカルシウム Ca の方が圧倒的に有利なので ナトリウムと水の反應: 2Na 2H2O → 2NaOH H2 高校化學では、Li〜Naは常温の水と、Mg〜Alは高温・高壓の水と反應することを習ふ。
酸化ナトリウムと水の反応について 酸化ナトリウムを水に加えた場合の反応は以下でいいのでしょうか? na2o → 2na^ + o^2 h2o → h^ + oh^ na2o h2o → 2naoh また同じ反応がリチウム、カリウムでも起こるのでしょうか?したがって、中和反応とは、水 h 2 o よりも酸性度が強い物質と水 h 2 o よりも塩基性度が強い物質の反応であると定義することにします。 また、硫酸 H 2 SO 4 と硝酸 HNO 3 をそれぞれ 1 mol だけ完全に中和するのに必要な水酸化ナトリウム NaOH は、それぞれ 1 mol および 2 mol になります。 しかし水酸化ナトリウムに関しては、必ず学習します。 その理由として反応しやすいこともあるでしょう。 例えば ・二酸化炭素と反応して、炭酸ナトリウムと水を生じます。 ・硫酸銅水溶液に加えると、水酸化第二銅と硫酸ナトリウムになります。
ナトリウムを水に入れると白煙が発生したのですが、 これは水酸化ナトリウムが水に溶けて霧状になっていると、考えました。 先生にこの煙を吸い込むとどんな感じだったか、また この時、のどではどんな反応が起きているかを考えてくるように言われ ナトリウムと水の化学反応式は 2Na2H2O→2NaOHH2 なんですけど、解き方と理由が知りた ひらたくいうと、水に何かを溶かすと熱が発生するという反応です(塩化ナトリウムなど吸熱するものもあります) そして水酸化ナトリウムはこの水和熱が非常に大きく445 kJ mol−1もの熱を発生します。




Na単体と水との反応 Youtube



酢酸 と 水 酸化 ナトリウム の 中 和 反応 式 食酢の中和滴定実験と考察
金属の反応(酸化と還元) (1) ナトリウムと水の反応 ナトリウム・Naは、 酸化され、陽イオン・Na+になる。①式 2Na → 2Na+ + 2e- 水・H2Oは還元され、 水素・H2と水酸化物イオンOH -を生化学反応式 2 CuO + C → 2 Cu + CO2 化学変化6 炭酸水素ナトリウムとうすい塩酸が混ざる と,二酸化炭素が発生し,塩化ナトリウムと 水ができる。 化学反応式 NaHCO3 + HCl → NaCl + CO2 + H2O 化学変化7 炭酸水素ナトリウムを熱分解すると,炭酸ナ③ 酸化炭素反応塔に導入した酸化炭素の量を精密に制御する。加圧分解した反応液に 残留した未反応の水酸化ナトリウムは、メタホウ酸ナトリウムから四ホウ酸ナトリウムへ の転換反応が終えた後、酸化炭素と反応して炭酸ナトリウムを生成する。



気体に関する化学変化
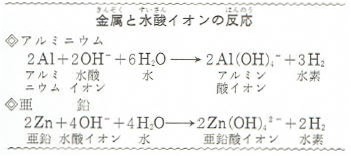



水酸化ナトリウムの性質 用途とは わかりやすく解説 科学をわかりやすく解説
高校化学の実験。米粒大のナトリウムを水で湿らせた濾紙の上に置くと、激しく反応し発火。Reaction of sodium with waterにして行なった 反応装置をセットし,空 気を流しておき,反 応 器に所定温度まで熱したチオ硫酸ナトリウム溶液(40Smg・ atom/Z)1400mZを 注ぎ,水 銀レギュレーターにより,温 度を調 節した この反応液に約18%の 過酸化水素5m∫ を注入し,25ナトリウムNaを水H2Oに入れると、水酸化ナトリウムNaOHと水素H2を生じる。 の化 Clear ナトリウムNaを水H2Oに入れると、水酸化ナトリウムNaOHと水素H2を生じる。 の化学反応式が分かりませ




ナトリウムと水の反応 らくらく理科教室




アルカリ 水酸化ナトリウム 水酸化カリウム
とした.対向型ナトリウム-水 反応場では,反応21:NaH 2 O → NaOHHが主となり反応が進行する.反応 21はナトリウムと水蒸気の重なり部 分で進行しており,生成される反応生成物が下側への流れによりナトリウムプール側に広がる分布を形成する. 塩酸と水酸化ナトリウムを反応させると、塩化ナトリウムと水ができました。 これを言い換えると、「 中和反応で酸と塩基が反応すると、塩水温が40℃を超えると水素が自然発火するので危険である。 エチルアルコールとは水素を発生して反応し,ナトリウムエトキシドNaOC 2 H 5 を生ずるが,-48℃以下では作用しない。
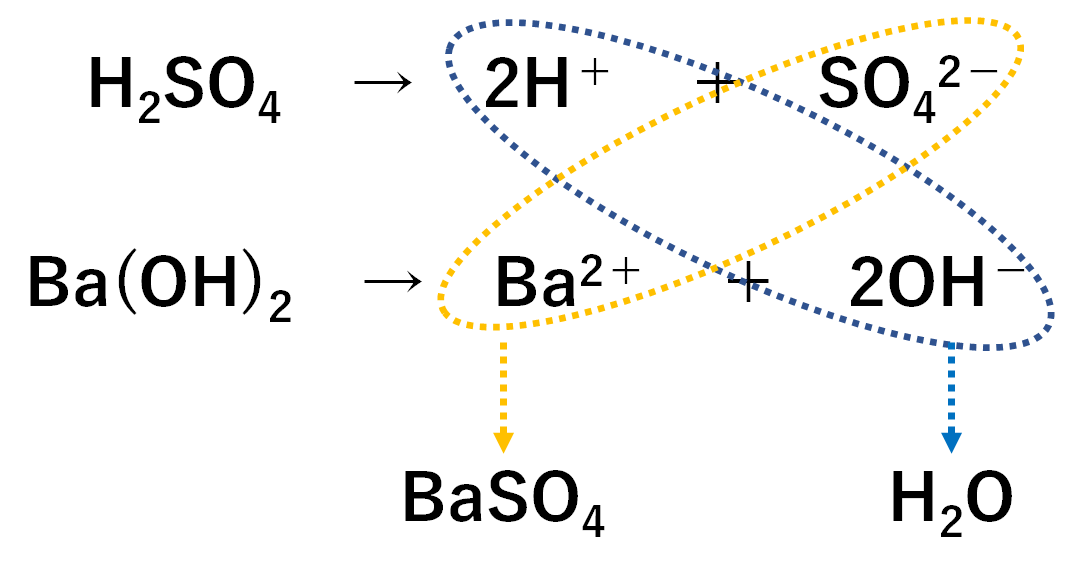



中3化学 中和反応 中学理科 ポイントまとめと整理



金属ナトリウムが水と反応するのはなぜですか 水酸化ナトリウムと水素が Yahoo 知恵袋
熱分解の生成物である炭酸ナトリウムNa 2 CO 3 と反応物である炭酸水素ナトリウムNaHCO 3 は,ともに白色の粉末ですね。 水に対する溶解性と,水溶液の液性が異なりましたね。 アルカリ金属は水$\ce{H2}$と反応して水酸化物となる.ナトリウム$\mrm{Na}$やカリウム$\mrm{K}$は激しく反応するので,注意が必要である. 保存方法 このように,アルカリ金属は非常に反応性に富むため,保存方法には気をつける必要があり, アルカリ金属は石油中に保存することになっています.禁水、泡消火剤、塩化ナトリウム以外の粉末消火剤 特有の危険有害性 激しい反応と火災の発生の危機があるため、水と接触させないこと。 水と接触すると爆発性ガス及び熱が放出される。 下水溝に流れ込むと火災、爆発の危険がある。




鉄と水酸化ナトリウムが反応しないのはなぜですか Clear




高校化学 水酸化アルミニウムの性質 映像授業のtry It トライイット
二酸化炭素がアレニウス塩基である水酸化ナトリウムの水溶液にたくさん溶けるのは、水酸化ナトリ ウム水溶液中のoh− と、二酸化炭素の電離で生じるh が中和して h oh− −→ h 2o 水が生じるからであると、中和反応で説明することも可能である。つまり 水素化ナトリウムのクエンチ・後処理方法 水素化ナトリウムはとても反応性が高いので、大量に未反応のNaHがあるときは水を加えてはいけません。 クエンチは氷浴で冷却しながらメタノール、エタノール(イソプロパノール)を滴下して加えます。 「動 画」ナトリウムと水との反応 Naの場合は、水と激しく反応したのち、水溶液は水酸化ナトリウムとなるため、フェノールフタレイン溶液の滴下によって赤紫色を呈します。




ナトリウム Sodium 食塩やベーキングパウダーに使用 Chem Station ケムステ



第141章 課題研究ii




アルカリ金属の実験準備 なんとなく実験しています




1995 5040号 塩化ナトリウムの工業用の水溶液の製造方法並びに水酸化ナトリウム水溶液の電気分解による製造 炭酸ナトリウムの製造及び塩化 ナトリウム結晶の製造のためのこうして得られた塩化ナトリウム水溶液の使用 Astamuse




高校化学 酢酸ナトリウムの加水分解 映像授業のtry It トライイット
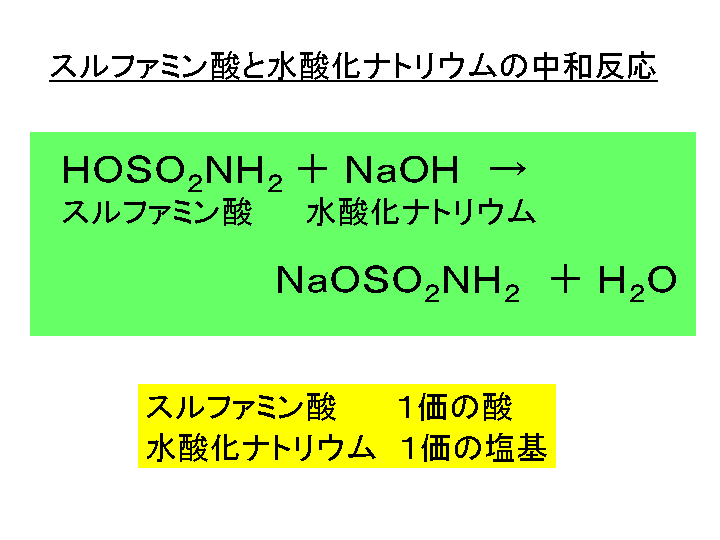



酢酸 と 水 酸化 ナトリウム の 中 和 反応 式 食酢の中和滴定実験と考察




炭酸水素ナトリウムを水に溶かした際に生じる炭酸イオンの濃度は 次の 化学 教えて Goo




高校理論化学 融解塩電解 溶融塩電解 ナトリウムna アルミニウムalの精錬 受験の月
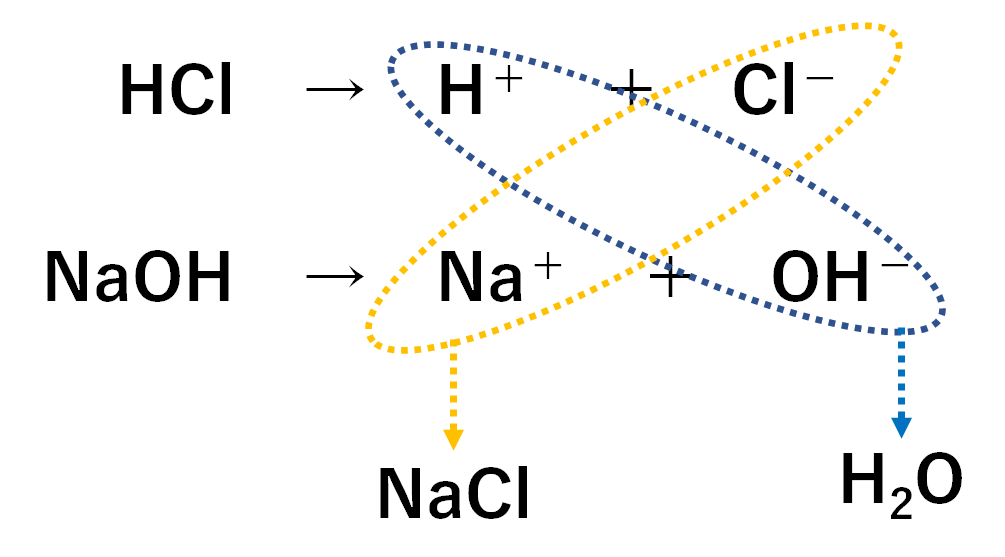



中3化学 中和反応 中学理科 ポイントまとめと整理
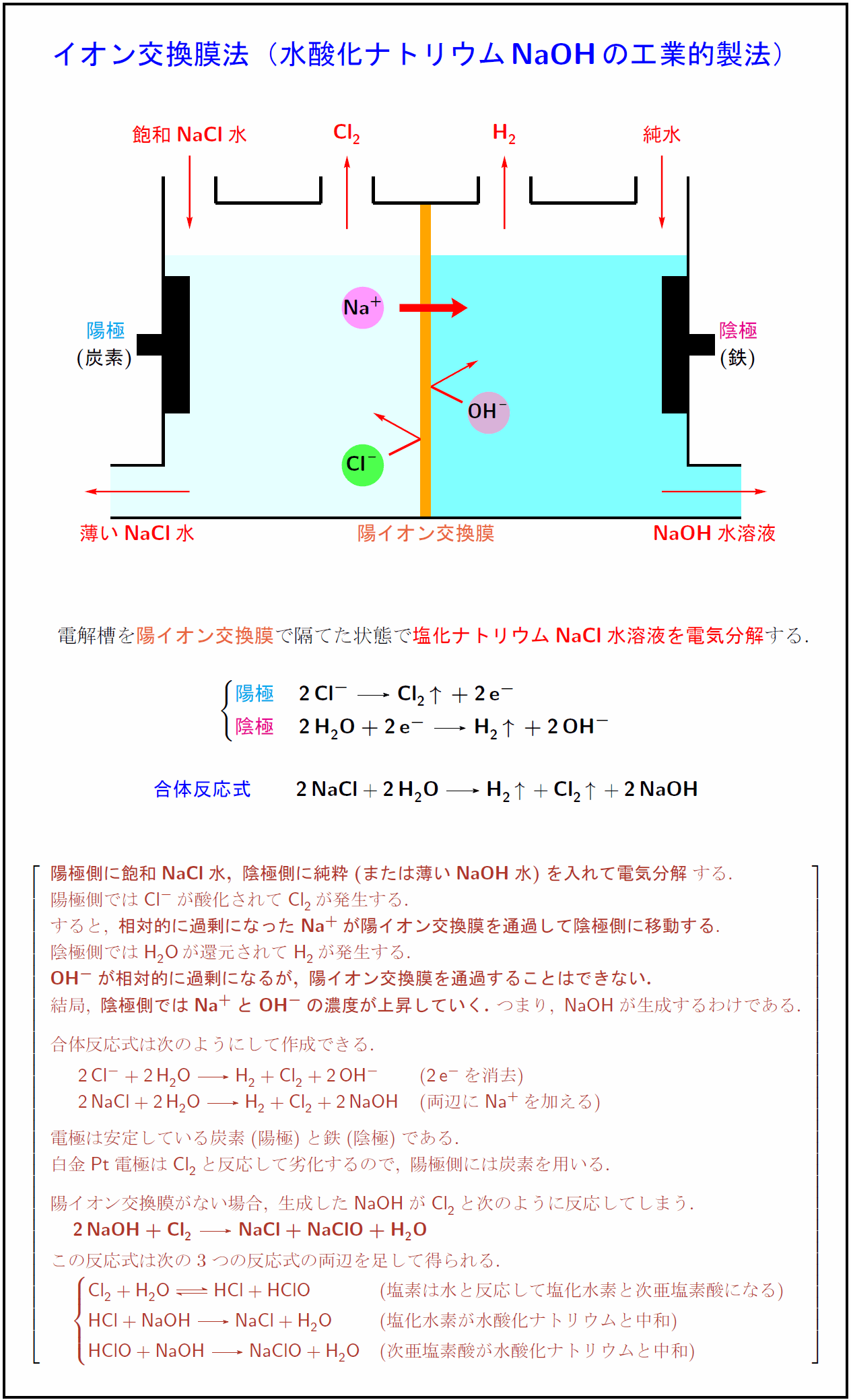



高校理論化学 イオン交換膜法 水酸化ナトリウムnaohの工業的製法 受験の月
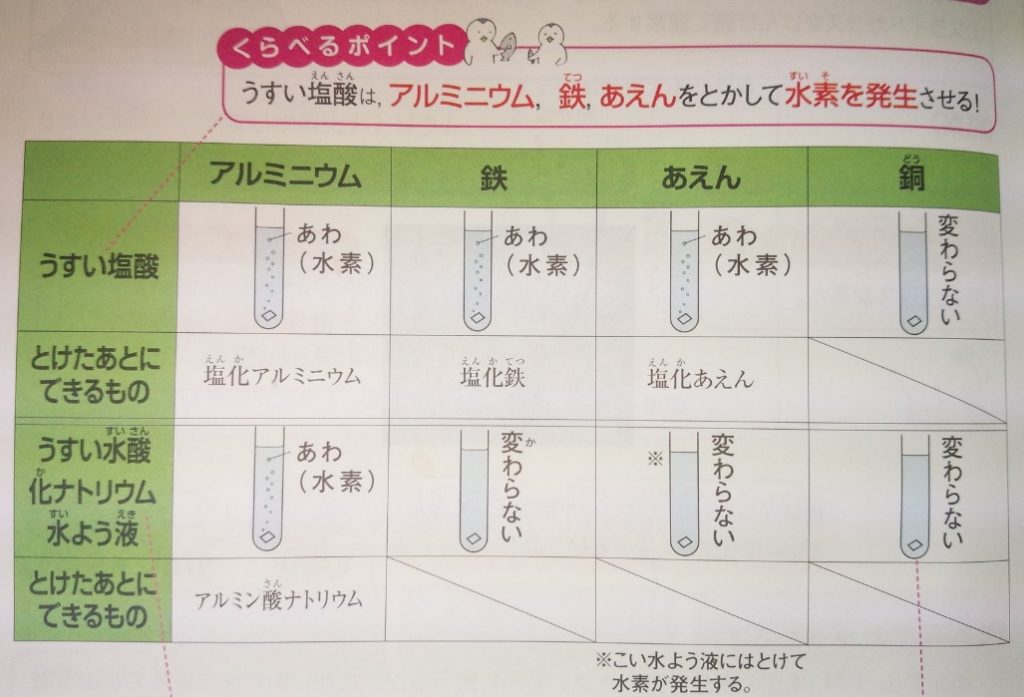



水溶液と金属の反応 塩酸 水酸化ナトリウム 中性は金属が溶けない




酢酸 と 水 酸化 ナトリウム の 中 和 反応 式




アルミニウムと水酸化ナトリウム水溶液の反応 化学がちょっとだけ好きな社労士



塩酸 と 水 酸化 ナトリウム を 混ぜる と




4 10ml 73ml Descubre Como Resolverlo En Qanda



酸と塩基が中和するときの科学反応式 よくわかりません 回答お願い Yahoo 知恵袋
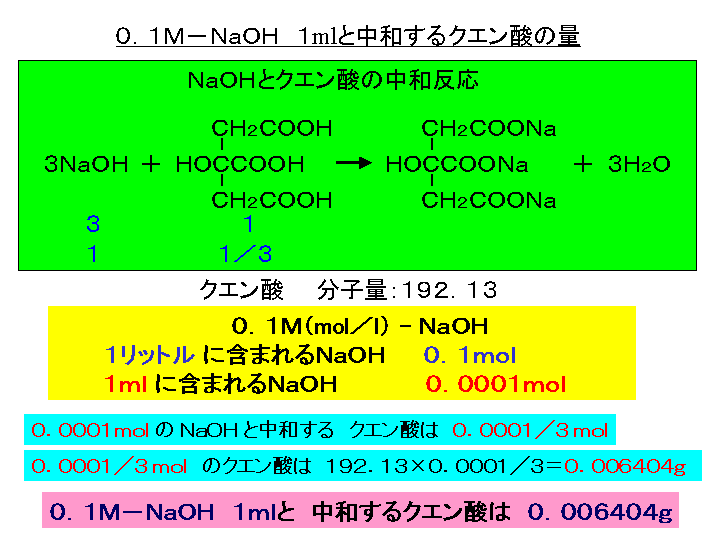



食品中の有機酸の定量 中和滴定




Left 3right O 1 2left N Descubre Como Resolverlo En Qanda



水酸化ナトリウムの溶解度




A cm3 Btb A10cm Descubre Como Resolverlo En Qanda




水 酸化 ナトリウム 電離 式




中性化 株式会社月形 公式ホームページ




化学基礎 中和の化学反応式なんですけど 解き方が全く分かりません Clear




水 酸化 ナトリウム 分子量
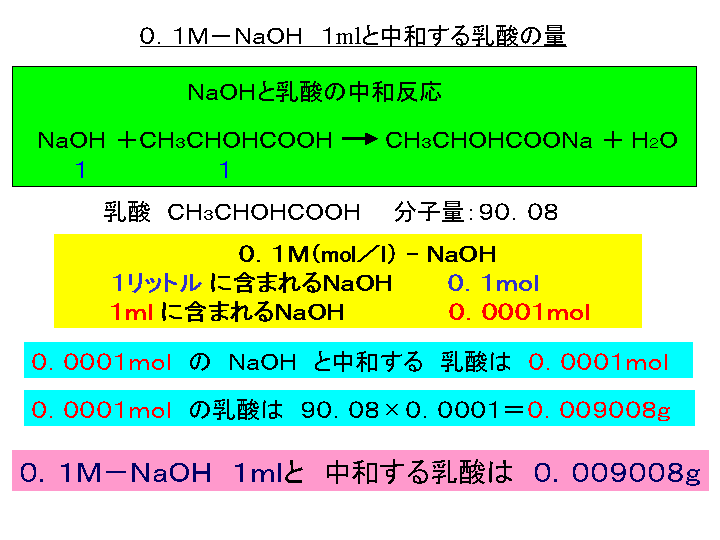



食品中の有機酸の定量 中和滴定



栃木県立真岡高等学校




高校化学 水酸化亜鉛の反応 映像授業のtry It トライイット



図 13 ナトリウム 水反応収納設備への閉止板取付




番を教えてください Clear
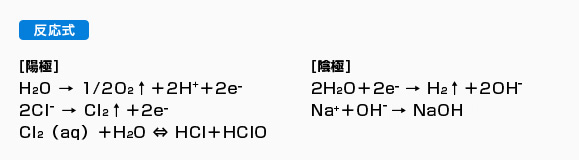



電解水 の基礎知識 電解水生成装置 ヘルス ソリューション 事業 製品案内 興研株式会社



実験12 塩酸と水酸化ナトリウムの中和反応 中学校理科の授業記録 化学3年 01年度 Taka




過不足のある化学反応の問題を解くコツと必ず書くべき図 保存版




食塩水の電気分解における電極での反応式 イオン式 陽極で塩素が発生し 陰極で水素が発生する理由




反応熱 Aqって何ですか 化学 定期テスト対策サイト
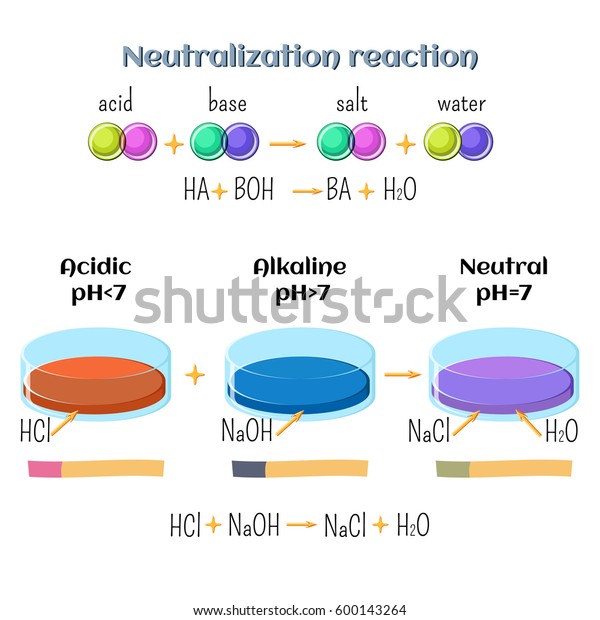



酸塩基 塩酸と水酸化ナトリウムの中和反応 化学反応の種類 第6部7部 子供向けの教育化学 フラットスタイルのカートーンベクターイラスト のベクター画像素材 ロイヤリティフリー




頻出 化学反応式 16 化学がちょっとだけ好きな社労士



予備校で酸化アルミニウムからテトラヒドロキシドアルミン酸ナトリウムの化 Yahoo 知恵袋




中学 高校化学 アルカリ金属と水の反応 Irohabook
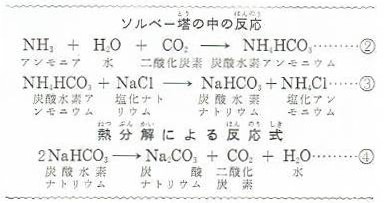



炭酸ナトリウムの製法とは わかりやすく解説 科学をわかりやすく解説




H C O Na Cl R と水酸化ナトリウムnaoh の中和反応を化学反応式で表すと 次式のように




番を教えてください Clear




1 025 Mol1 L ml 0 N Descubre Como Resolverlo En Qanda




水 酸化 ナトリウム 潮解 性 Article
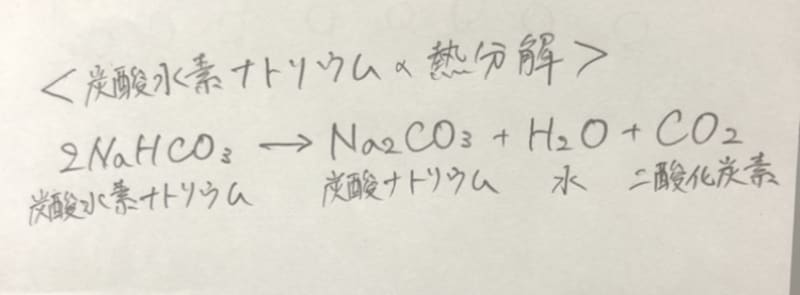



炭酸水素ナトリウムの化学反応式を教えてください アンサーズ




写真の問題について質問です なぜ塩化バリウムは水酸化ナトリウムと反応せず 炭酸ナトリ Clear




水 酸化 ナトリウム 分子量




Periodic Table Na




酢酸 と 水 酸化 ナトリウム の 中 和 反応 式 食酢の中和滴定実験と考察




16 Descubre Como Resolverlo En Qanda



中和について 固体 液体 気体 の達人



アルカリ金属の実験
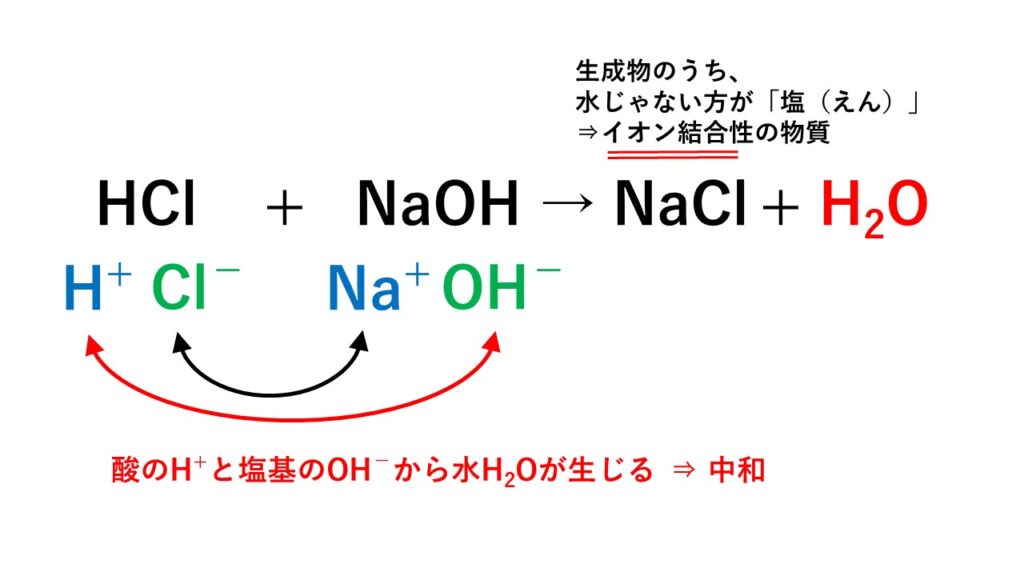



5分でわかる 中和反応とは 化学反応式と計算問題の解き方 練習問題付き サイエンスストック 高校化学をアニメーションで理解する



フルーツ 前方へ 美人 炭酸 水素 ナトリウム 炭酸 水 Cb Music Jp
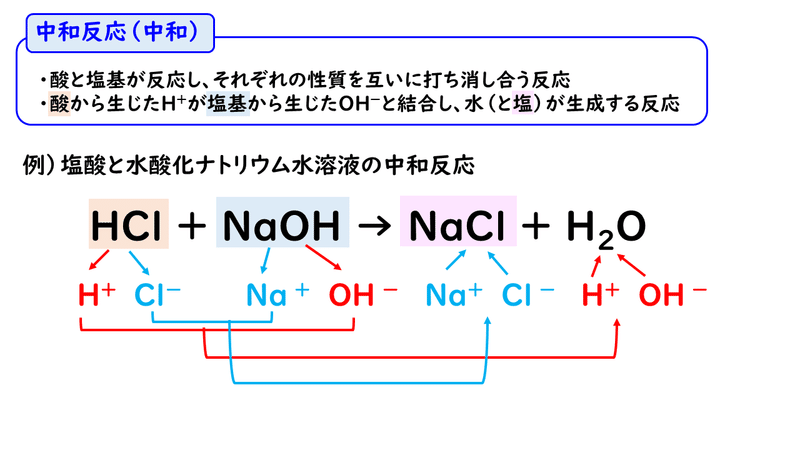



6 3 中和反応 おのれー Note




高校化学 亜鉛の性質 練習編 映像授業のtry It トライイット




ナトリウムと水 Youtube




希硫酸の陽極と水酸化ナトリウム水溶液の陽極の違いを教えて下さい Clear



アルカリ金属の爆発の秘密が明らかに Nature ダイジェスト Nature Portfolio




炭酸 水素 ナトリウム 塩酸 炭酸ナトリウムによる塩酸の中和滴定
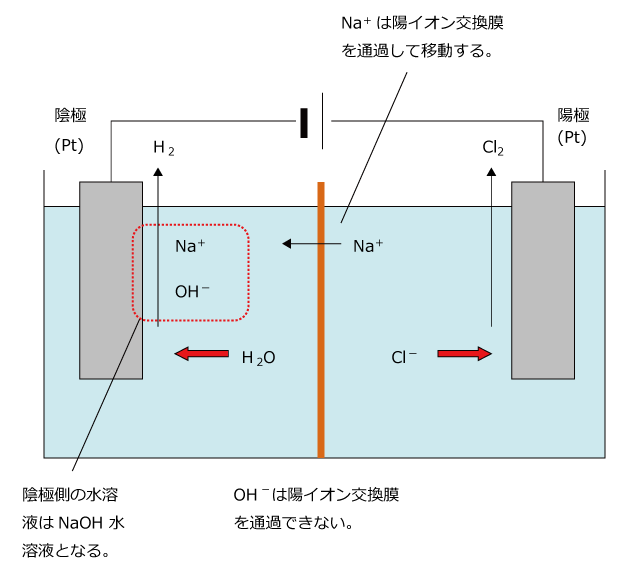



化学講座 第28回 電気分解 さまざまな電気分解 私立 国公立大学医学部に入ろう ドットコム



高校入試の理科に出やすい問題 化学式編 個別指導学習塾開成館アカデミー桂川




科学 化学 食塩でお馴染みだけど爆発もする ナトリウム Alis




化学工業の歴史1 無機 有機化学工業の基盤成立 化学工業の基礎知識2 ものづくり まちづくり Btob情報サイト Tech Note



化学工場爆発 消防隊が放水して再び爆発 雨漏り原因 金属ナトリウムと激烈反応 中国メディア サーチナ
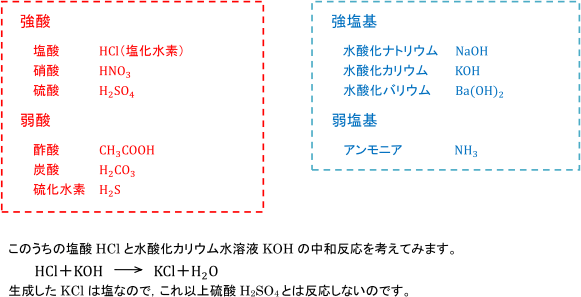



中和反応と塩 塩化カリウムと硫酸が反応しないのはなぜですか 化学基礎 定期テスト対策サイト
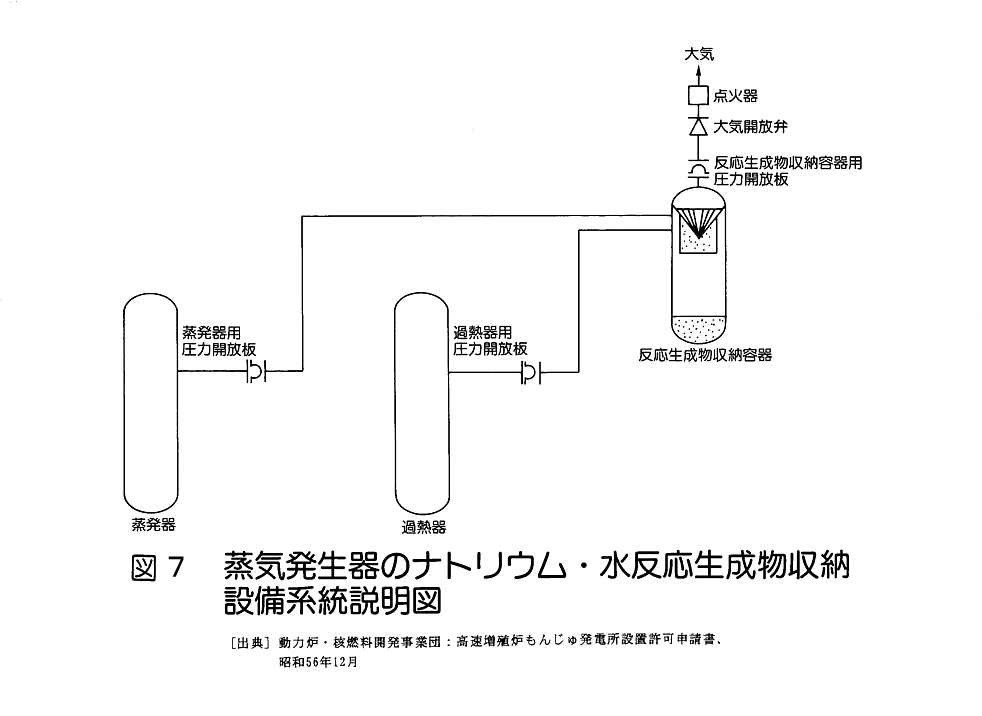



蒸気発生器のナトリウム 水反応生成物収納設備系統説明図




酢酸 と 水 酸化 ナトリウム の 中 和 反応 式 酸と塩基 中和反応



マイクロスケール水の電気分解




高校化学 酢酸ナトリウムの加水分解 映像授業のtry It トライイット




酢酸 と 水 酸化 ナトリウム の 中 和 反応 式




水酸化ナトリウム 電気分解 化学反応式




化学 金属ナトリウムと水の反応 Youtube




中3化学 水の電気分解 中学理科 ポイントまとめと整理




なぜ水酸化ナトリウムが先に反応するんですか Clear




化学実験 アルカリ金属と水の反応 取り扱い注意 危険 Youtube




酢酸 と 水 酸化 ナトリウム の 中 和 反応 式 食酢の中和滴定実験と考察



50 グレア ナトリウム 水 反応 100 イラスト




水の電気分解の仕組み 反応式 陽極 陰極での反応式 水酸化ナトリウムを入れる理由は




中和と塩




1 025 Mol1 L ml 0 N Descubre Como Resolverlo En Qanda
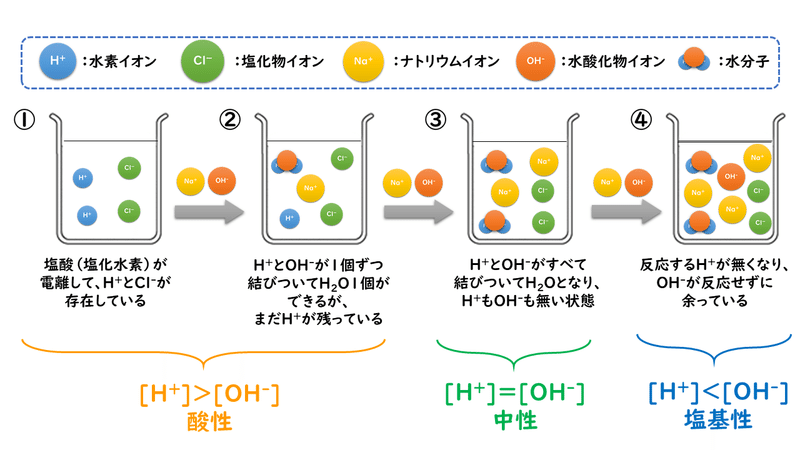



6 3 中和反応 おのれー Note




高校化学 Naohとna Co の性質 映像授業のtry It トライイット



水酸化ナトリウムの性質と反応 ネットdeカガク



高校入試の理科に出やすい問題 化学式編 個別指導学習塾開成館アカデミー桂川



2 o 問1 次の各化学反応式に係数を入れよ




塩酸 水 酸化 ナトリウム



コメント
コメントを投稿